Презентация На Тему Получение Серной Кислоты
- Презентация На Тему Производство Серной Кислоты Контактным Способом
- Презентация На Тему Производство Серной Кислоты
Презентация к уроку на тему Серная кислота +. Для получения серной. Презентация на тему «Производство серной кислоты». Выполнила: Ученица 11 французского класса Александрова Валентина. Серная кислота H2SO4: сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6). Тяжёлая маслянистая жидкость без цвета и запах а в технике серной кислотой называют её смеси как с водой, так и с серным ангидридом SO3. Основные стадии получения серной кислоты: Обжиг сырья с получением SO2 Окисление SO2 в SO3 Абсорбция SO3 В промышленности применяют два метода окисления SO2 в производстве серной кислоты: контактный — с использованием твердыхкатализаторов(контактов) нитрозный — с оксидами азота. Feb 11, 2017 - Чтобы посмотреть презентацию с оформлением и слайдами, скачайте ее файл. Производство серной кислоты Подготовка к ЕГЭ11.
Кислоты Лакмус будет в них краснеть, Растворяться – цинк и медь. А мелок в них, посмотри, В миг пускает пузыри! И опасны для работы Эти жгучие кислоты. Выполнила: Семёнова Елена Сергеевна КГУ «школа-лицей № 4 акимата г. Рудного» Содержание 1). Формулы кислот. Классификация кислот.
Физические свойства. Способы получения. Химические свойства.
Техника безопасности при работе с кислотами. Вопросы для повторения. Формулы кислот. Кислотами называются сложные вещества, состоящие из атомов водорода, способных замещаться на атомы металлов и кислотных остатков. НАЗВАНИЕ КИСЛОТЫ ФОРМУЛА СОЛЯНАЯ HCl АЗОТНАЯ HNO 3 СЕРНА Н 2 SO 4 УГОЛЬНАЯ H 2 CO 3 ФОСФОРНАЯ H 3 PO 4 КРЕМНИЕВАЯ H 2 SiO 3 ЙОДОВОДОРОДНАЯ HI БРОМОВОДОРОДНАЯ HBr СЕРОВОДОРОДНАЯ H 2 S БОРНАЯ H 3 BO 3 СЕРНИСТАЯ H 2 S К содержанию Классификация кислот По наличию или отсутствию кислорода в своём составе кислоты делятся на кислородсодержащие и бескислородные.
4, г); — прихватывают порог газовой сваркой в указанных на рис. 4, г стрелками местах; — навешивают дверь и контролируют штангенциркулем установку порога по зазорам (рис. 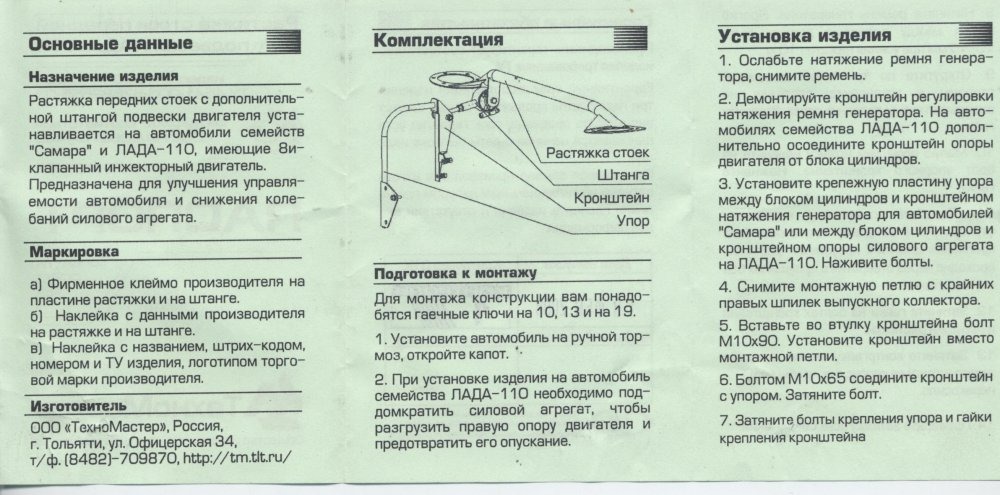
Кислоты бескислородные кислородсодержащие HCl HNO 3 HBr H 2 SO 4 H 2 S H 2 SiO 3 В состав кислот входит различное число атомов водорода. Если в состав кислоты входит 1 атом водорода, она называется одноосновной, если 2 атома водорода - двухосновной и т.д. Кислоты одноосновные двухосновные трёхосновные HCl HBr HI H 2 SO 4 H 2 CO 3 H 2 SO 3 H 3 PO 4 H 3 BO 3 К содержанию Физические свойства.
Многие кислоты – это бесцветные жидкости, например серная H 2 SO 4, соляная HCl, азотная HNO 3. Известны также твёрдые кислоты: борная Н 3 ВО 3. Почти все кислоты растворимы в воде. Пример нерастворимой кислоты – кремниевая H 2 SiO 3.
Признаком, характеризующим кислоты, является кислый вкус. К содержанию Способы получения кислот Взаимодействие кислотных оксидов с водой.
Взаимодействие водорода с неметаллом. Взаимодействие кислот с солями. CO 2 + H 2 O H 2 CO 3 SO 3 + H 2 O H 2 SO 4 P 2 O 5 + 3H 2 O 2H 3 PO 4 H 2 + Cl 2 2HCl (при растворении в воде) 2NaCl + H 2 SO 4 Na 2 SO 4 + 2HCl К содержанию Видео Взаимодействие хлора с водородом Видео Получение угольной кислоты Химические свойства 1). Действие кислот на растворы индикаторов. (от латинского indicator – указатель) Вещества, которые под действием растворов кислот и щелочей изменяют свой цвет, называются - индикаторами.
К ним относятся: лакмус, фенолфталеин, метиловый оранжевый, универсальный и некоторые другие. Индикатор цвет индикатора в среде Лакмус кислой Фенолфталеин красный щелочной Метиловый нейтральной синий бесцветный фиолетовый малиновый оранжевый розовый бесцветный жёлтый оранжевый 2). Характерным свойством кислот является их взаимодействие с металлами.
При проведении этих реакций нужно руководствоваться рядом активности металлов, который вывел русский учёный Н.Н. Металлы располагаются в соответствии с их химической активностью: Li K Na Ca Mg Al Zn Fe Ni Sn Pb H 2 Cu Hg Ag Pt Au Вытесняют водород из кислот, Водород из кислот исключение - азотная кислота HNO 3 не вытесняют. Вместо водорода выделяются другие газы. Li K Na Ca Mg Al Zn Fe Ni Sn Pb H2 Cu Hg Ag Pt Au. Активность металлов растёт в ряду справа налево. Самый активный металл – Li, самый пассивный – Au.
Руководство по эксплуатации фольксваген поло хэтчбек скачать бесплатно. В начале этого ряда расположены активные металлы - Li, K, Na, Ca – они могут легко вытеснить водород из воды. Zn + 2HCl ZnCl 2 +H 2 Mg + H 2 SO 4 MgSO 4 + H 2 HCl + Cu реакция не идёт Видео Взаимодействие кислот с металлами 3). Взаимодействие с основными оксидами. Оксид Ме + кислота соль + вода CuO + H 2 SO 4 CuSO 4 + H 2 O 4).
Взаимодействие с основаниями. Реакция нейтрализации. Основание + кислота соль + вода NaOH + HCl NaCl + H 2 O 5).
Взаимодействие с солями. Реакция возможна тогда, когда может образоваться осадок или газ. BaCl 2 + H 2 SO 4 BaSO 4 + 2HCl CaCO 3 + 2HCl CO 2 + H 2 O + CaCl 2 6). При нагревании некоторые кислоты разлагаются с образованием кислотного оксида и воды. H 2 SiO 3 SiO 2 + H 2 O К содержанию Техника безопасности при работе с кислотами 1 ). Кислоты нельзя пробовать на вкус, т.к.
Они вызывают ожоги и отравления. При работе с кислотами, особенно концентрированными, пользоваться резиновыми перчатками. Нельзя вдыхать пары кислот.
Презентация На Тему Производство Серной Кислоты Контактным Способом
При разбавлении концентрированных кислот, нужно приливать кислоту в воду, а не наоборот, при постоянном помешивании. При разбавлении кислот необходимо пользоваться только тонкостенной химической или фарфоровой посудой.
При попадании кислоты на кожу, промыть под струёй прохладной воды, при необходимости на обожжённое место наложить примочку из 2% раствора питьевой соды. При отравлении кислотой: выпить 5-6 стаканов тёплой воды и вызвать рвоту, затем выпить столько же раствора питьевой соды и снова вызвать рвоту. Затем сделать 2 промывания желудка чистой тёплой водой. Общий объём не менее 6 л. Инструкция по сборке стенки магия. Обратиться к врачу. По быстроте действия и по скорости разрушения тканей тела кислоты располагаются в следующем порядке, начиная с более сильных: «царская водка» – смесь концентрированных HNO 3 и НСl 1:3 по объёму, HNO 3, H 2 SO 4, HCl, уксусная, щавелевая и т.д. Дымящиеся кислоты раздражают слизистые оболочки дыхательных путей и глаз.
К содержанию Вопросы для повторения 1). Сложное вещество, состоящее из атома водорода и кислотного остатка называется – 2). Вещества, изменяющие цвет в растворах кислот называются – 3).
Какой цвет лакмуса в кислоте – 4). Самый активный Ме в ряду активности металлов – 5). Самый пассивный Ме в ряду активности металлов – 6). Фамилия русского учёного составившего ряд активности Ме – 7). Как называется эта кислота H 2 SiO 3 - кислота индикаторы красный Li Au Н.Н.Бекетов кремниевая.

Презентация На Тему Производство Серной Кислоты
Слайд 2 Исторические сведения Серная кислота известна с древности. Первое упоминание о кислых газах, получаемых при прокаливании квасцов или железного купороса «зеленого камня», встречается в сочинениях, приписываемых арабскому алхимику Джабир ибн Хайяну. Позже, в IX веке персидский алхимик Ар-Рази, прокаливая смесь железного и медного купороса (FeSO4.7H2O и CuSO4.5H2O), также получил раствор серной кислоты.
Этот способ усовершенствовал европейский алхимик Альберт Магнус, живший в XIII веке. Молекула серной кислоты по Дальтону:. Слайд 6 Токсическое действие Серная кислота и олеум — очень едкие вещества. Они поражают кожу, слизистые оболочки, дыхательные пути (вызывают химические ожоги).
При вдыхании паров этих веществ они вызывают затруднение дыхания, кашель, нередко — ларингит, трахеит, бронхит и т. д. ПДК аэрозоля серной кислоты в воздухе рабочей зоны 1,0 мг/м³, в атмосферном воздухе 0,3 мг/м³ (максимальная разовая) и 0,1 мг/м³ (среднесуточная). Поражающая концентрация паров серной кислоты 0,008 мг/л (экспозиция 60 мин), смертельная 0,18 мг/л (60 мин). Класс опасности II. Аэрозоль серной кислоты может образовываться в атмосфере в результате выбросов химических и металлургических производств, содержащих оксиды S, и выпадать в виде кислотных дождей. Слайд 7 Серную кислоту применяют: в производстве минеральных удобрений; как электролит в свинцовых аккумуляторах; для получения различных минеральных кислот и солей; в производстве химических волокон, красителей, дымообразующих веществ и взрывчатых веществ; в нефтяной, металлообрабатывающей, текстильной, кожевенной и др.
Отраслях промышленности; в пищевой промышленности — зарегистрирована в качестве пищевой добавки E513(эмульгатор); в промышленном органическом синтезе в реакциях: дегидратации (получение диэтилового эфира, сложных эфиров); гидратации (этанол из этилена); сульфирования (синтетические моющие средства и промежуточные продукты в производстве красителей); алкилирования (получение изооктана, полиэтиленгликоля, капролактама) и др. Слайд 10 Основные стадии получения серной кислоты: 1) Обжиг сырья с получением SO2 2) Окисление SO2 в SO3 3) Абсорбция SO3 В промышленности применяют два метода окисления SO2 в производстве серной кислоты: контактный — с использованием твердых катализаторов (контактов), и нитрозный — с оксидами азота. Из минерала пирита на катализаторе — оксиде ванадия (V). 4FeS2 + 11O2 = 2Fe2O3 + 8SO2 2SO2 + O2 (V2O5) → 2SO3 SO3 + H2O → H2SO4 Нитрозный метод получения серной кислоты SO2 + NO2 → SO3 + NO↑. 2NO+O2 → 2NO2 При реакции SO3 с водой выделяется огромное количество теплоты и серная кислота начинает закипать с образованием 'туманов' SO3 + H2O = H2SO4 + Q Поэтому SO3 смешивается с H2SO4, образуя раствор SO3 в 91% H2SO4 - олеум. Слайд 18 Заключение В производстве H2SO4 соблюдены основные направления развития химической промышленности: Технология малоотходная – переход сырья в целевой продукт достигает 99%.
Энергосберегающее, так как процесс обеспечивает сам свое энергосбережение. Эта химическая технология обладает рядом функций: Рациональное использование сырья и энергии. Масштабность и дешевизна.
Поскольку процесс непрерывен, он обладает рядом достоинств: Большое количество продукта с 1 объема аппарата – высокая интенсивность процесса. Исключение потерь тепла из-за термодинамичности – нагрев – охлаждение. Легкость автоматизации. Также процесс учитывает основные принципы химической технологии: Наибольшая интенсивность процесса; Наилучшее использование сырья; Наибольшее использование энергии.